刘亮医生的科普号
- 精选 微创胰腺手术的未来
腹腔镜或手术机器人的应用已经风靡全球,毫无疑问这是未来的一个趋势。然而,这个未来是多久呢?刚刚结束了今天(元宵节)的手术,我就被来源于欧洲胰腺中心的一项重磅报道震惊到了:今晨(2024-2-24凌晨)
 刘亮 主任医师 上海中山医院 普外科185人已读
刘亮 主任医师 上海中山医院 普外科185人已读 - 精选 Crit Rev Oncol Hematol|复旦中山医院揭示早发性癌症的内在共同生物学和临床特征
癌症导致的死亡居于所有死亡原因之首,是人类延长寿命的最大障碍。癌症不仅给个人,家庭,同时也给整个社会卫生保健系统带来沉重负担。癌症既往被认为是种“老年病”,与年龄的增长密切相关。然而,现今越来越多中年人,甚至青壮年也不幸“中招”,沉重的现实令人不禁担忧是否明天厄运就会降临在自己身上。2023年9月1日,复旦大学附属中山医院胰腺外科刘亮团队在国际知名期刊《CriticalReviewsinOncology/Hematology》上在线发表题为“Biologicalandclinicalimplicationsofearly-onsetcancers:Auniquesubtype”的综述文章,系统性总结了“早发性癌症”作为一种独特的癌症亚型内在共通的临床和生物学特征。“早发性癌症”这一说法最早来源于结直肠癌,指发生于50周岁以下人群的结直肠癌,而今这一概念被包括胰腺癌,胃癌,乳腺癌在内的众多上皮源性恶性肿瘤所使用。就胰腺癌而言,发病年龄<50岁被定义为“早发性胰腺癌”。上皮源性恶性肿瘤的高发年龄一般为65-70周岁,尤其胰腺癌由于常见发病年龄超过65岁,常常被称为“老年性肿瘤”。但现今的临床实践中,越来越多的能见到许多年轻患者,这些患者的临床和生物学表现也与常见的癌症患者有所不同。因此,深入了解这部分患者内在的临床和分子生物学特征很有必要,可能会对后续临床诊疗具有指导意义。图1.2010-2019年50周岁以下人群不同癌症的发病率趋势变化在这篇综述中,刘亮团队以结直肠癌,胰腺癌,乳腺癌,胃癌等发病率与死亡率较高的上皮源性恶性肿瘤为例,分析总结了早发性癌症内在的共性与个性。早发性癌症是指癌症的发病年龄较早,这一概念与一般癌症在全生命周期中的“晚发”相对。现在一般认为早发性癌症的年龄界线是50岁,通常较一般癌症肿瘤分化更差,恶性程度更高,也更早的出现侵袭转移。但由于早发性癌症患者体力状况较好,可以接受更积极的治疗策略或耐受毒性更大的化疗方案,治疗后的并发症也较少,长期生存并不明显劣于一般癌症。此外,早发性癌症的患者通常具有相似的流行病学风险因素,如吸烟、酗酒、肥胖、糖尿病及缺乏体力活动等。值得注意的是,早发性癌症的发病风险和暴露于风险因素的起始时间高度相关。例如,越早开始吸烟酗酒的年轻人患癌的风险越大,发生的年龄也越早。早发性癌症还通常具有显著的家族聚集性。近亲属中有一人患癌可将早发性癌症的发生概率提高2倍,若有两人患癌可提高3倍以上。一些特定的遗传改变如癌基因KRAS突变或DNA损伤修复基因BRCA突变亦可导致早发性癌症发生的风险明显增加。刘亮教授总结指出,为减少早发性癌症的发病率,需做到以下两点:一是要尽早的纠正不良的生活习惯,提倡健康饮食,合理锻炼,控制体重;二是针对有明显家族风险史的人群要尽早开展疾病筛查和基因检测,以检出潜在的早发性癌症患者。此外,早发性癌症作为一种独特的癌症亚型目前的针对性研究和临床试验还处于起步阶段,应全面开展针对早发性癌症患者诊疗的研究和临床试验,以延长这部分患者的预后和生存。复旦大学附属中山医院胰腺外科何韬宸博士、李剑昂博士、徐志航博士为本文共同第一作者。刘亮教授、王文权教授和浦宁医师为共同通讯作者。
 刘亮 主任医师 上海中山医院 普外科164人已读
刘亮 主任医师 上海中山医院 普外科164人已读 - 精选 与众不同的“壶腹周围癌”——六问六答
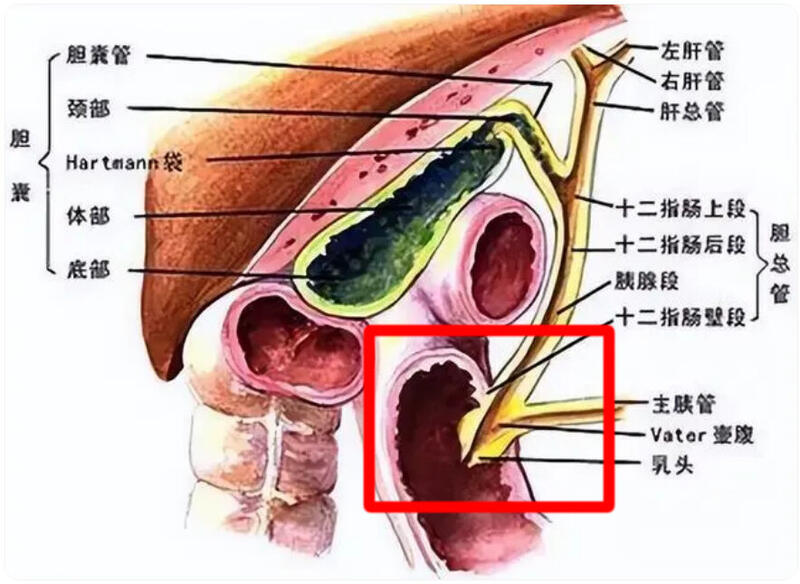
1, 壶腹周围癌的定义:答:壶腹周围癌起源于壶腹部2cm以内的范围,包括Vater壶腹、胆总管末端、胰管开口处、十二指肠乳头及其附近粘膜的癌。临床常见的为十二指肠乳头癌,胰头癌、胆总管下端癌。2,壶腹
 刘亮 主任医师 上海中山医院 普外科2031人已读
刘亮 主任医师 上海中山医院 普外科2031人已读 - 媒体报道 胰腺癌不再可怕!2021-胰腺癌综合诊治“曙光初现,任重道远”
胰腺癌是 “癌中之王”,死亡率高,治疗乏术。半个世纪以来,病人的5年生存率始终徘徊在5%左右,半数以上的病人在1年内死亡。然而,2020年美国国立卫生研究院(National Institutes o
刘亮 主任医师 上海中山医院 普外科6619人已读 - 医学科普 CA125在胰腺癌中的“特殊”临床价值——提示转移
CA125,是一个特异性提示卵巢癌诊断或疾病进展的肿瘤标志物,广泛应用于诸多妇科肿瘤如宫颈癌、宫体癌、子宫内膜癌等的诊断和随访。事实上,CA125在其它非妇科肿瘤如乳腺癌、胰腺癌、胃癌等也有应用。而对
刘亮 主任医师 上海中山医院 普外科7940人已读 - 医学科普 血清CA19-9是不是越低越好?——论“CA19-9阴性胰腺癌”的临床意义
CA19-9是迄今为止胰腺癌诊断敏感性最高,也是临床应用最为广泛的血清肿瘤学标记物。但实践中,我们常常碰到不少已经罹患并病理确诊的胰腺癌病人心存疑惑:其CA19-9并不高甚至很低,但为什么也确诊为胰腺
刘亮 主任医师 上海中山医院 普外科8186人已读 - 对微创手术在胰腺肿瘤中的推广应该抱有谨慎态度
跨入新世纪以来20年间,外科手术的进展当属腹腔镜或机器人辅助下的微创手术蓬勃开展。在各学术会议,各种宣传媒体,以及病人之间的“口口相传”中,目前均对微创手术倍加推崇。最近我在肿瘤学专业学术会议上发表了个人对此的一些看法,供大家参考,希望大家批评指正。1, 挑选合适的病人开展微创手术,绝不应该扩大适应症:由于微创手术高度依赖手术器械,主刀医生对手术野以及器官的感知程度容易出现偏差,因此目前绝大多数的外科医生在开展微创手术之前,对病人和疾病的选择非常严格:就病人而言,全身情况欠佳,过于肥胖等均不适合微创手术;就肿瘤而言,包绕大血管,侵犯多脏器等也不适合微创手术。换一句话来说,外科医生仅选择最有把握的病人开展微创手术。而不应该纯粹追求“小切口”,“为微创而微创”。在一切以病人安全或长期生存为考量的前提下,医生高度的责任心和控制力尤为重要。2, 挑选合适的肿瘤疾病开展微创手术,而不应该盲目进行。以胰腺肿瘤为例,目前针对微创技术的临床研究,虽然提示在手术安全性上有长足进步,但是对于肿瘤学获益(即对病人而言,至关重要的“生存”)却存在争论。几乎所有的研究结论均为“非劣效性”——即微创手术疗效“不逊色”于传统开放手术,而并非老百姓期望的优于或超过传统手术。在这样的情况下,经过严格“筛选”后的优势病例(微创)与不加挑选的普通病例(传统)进行比较,居然得不出优势结论,我们有什么理由,或者说有什么胆量敢在临床实践中盲目推广呢?3, 同样以胰腺癌实践为例,截止2020年底,国际ClinicalTrial网站上登记在研的与微创与传统开放手术比较的临床研究大约9项(很少),其中半数在中国。一方面说明我们国内的外科医生勇于尝试新事物,心灵手巧;但另一方面也反映世界范围内对胰腺恶性肿瘤开展微创手术仍然较为谨慎,特别日本,德国,美国的普及程度均明显落后于我国。国外发明的先进技术反而没在国外广泛推广,这一现状值得我们在临床创新中深思。
刘亮 主任医师 上海中山医院 普外科1199人已读 - 学术前沿 胰腺癌术前转化治疗的几点意见——因为专业所以规范,因为规范所以领先
胰腺癌是手术切除率最低的实体性肿瘤,通过“术前转化治疗”争取手术会是病人获得长期生存的希望,也是临床医生努力的重要方向。“术前转化治疗”(包括“新辅助治疗”)是胰腺癌综合诊治的主要内容,也是临床和基础研究领域的热点。目前术前转化治疗已在临床实践中深入人心,但仍有几个问题需要明确:1,实践对象:目前适合开展转化治疗的胰腺癌病人主要包括两部分人群:①肿瘤局部严重:如“交届可切除”:重要静脉被肿瘤包绕;和“局部进展”:动脉包绕或局部静脉切除后无法重建。②远处转移适度:仅少数转移性胰腺癌病人,如体力状态良好,合并寡转移灶,局部肿瘤可切除的病人有可能转化成功;而转移程度严重,范围较大的病人并不适合开展转化治疗。2,转化治疗策略的制定:2020年国内外指南扩充了胰腺癌转化治疗的手段,已由单一的化疗或化放疗向“化疗+放疗+靶向治疗+免疫治疗”等综合方式的扩展。治疗手段的增加,有望带来“1+1>2”的效果,为病人带来福音。但无论怎样,①治疗前病理结果的取得,②病人状态评价,③肿瘤组化及分子分析,④基因检测筛查等一系列评估是制定完善方案的必选项,缺一不可。3,转化治疗疗程的设定:依据胰腺癌中位进展时间分析,转化治疗时间初步设定为4个疗程。若客观缓解率高的病人,手术时间可以提前;反之延后。临床工作中,术前转化治疗时间延长至8-9个疗程以上才获得手术机会的病例并不罕见。4,如何评估术前转化治疗疗效?如何定义手术指证?最佳评判转化治疗疗效的方法仍然是病理学评价,但临床可操作性不强(既然决定手术,就不再安排重复的穿刺或活检)。目前临床判定标准主要在于:①病人状态良好,具有开展根治性手术的体力储备。②肿瘤稳定或不进展:术前转化治疗后,只要局部肿瘤不增大,远处转移不出现或不增加,就具有手术探查的条件,值得放手一搏。③血清学肿瘤标记物下降:临床实践表明,CA19-9下降超过50%,甚至降至正常,预后更佳。5,医患双方心理和体力准备同样重要:接受转化治疗后的拟根治性手术的胰腺癌,手术更大,风险更高。无论病人和家属,包括手术医生,都应该做好充分的心理和体力方面的准备。对病人或家属而言,需要对医生的绝对信任和应对风险的决心。对医生而言,要有迎难而上的决心和毅力,要有临危不乱的心理素质和高超的手术技能,更要有勇于承担风险的责任心。这几方面缺一不可。
刘亮 主任医师 上海中山医院 普外科1367人已读 - 医学科普 胰腺癌术后辅助治疗的几点思考——要不要做?如何做?
1,术后辅助治疗的必要性:目前无论国内或是国外指南,均推荐根治手术后的胰腺癌病人需要进一步接受以化疗为主的辅助治疗。主要考虑为:(1)肿瘤是一种系统性疾病。系统性疾病需要系统性诊治,是抗癌治疗的共识。没有任何一种治疗手段能够完全控制或消灭肿瘤,需要我们常常提及的“组合拳”或“鸡尾酒”新型策略。(2)以手术为例,外科医生往往切除的是肉眼可见的病灶;即使扩大切除,范围依然有限,不可能盲目扩张。对已经播散至全身血液,淋巴系统或腹腔内的隐匿性病灶或癌细胞,以手术为主的局部治疗往往无能为力。据保守估计,即使胰腺癌根治术后存在于人体内的残留癌细胞数量仍然可以达到惊人的1012(打个比方,这个数量的概念类似于目前一百倍的中国人口)。因此,进一步消灭这些播散至全身的游离癌细胞是防治术后复发的关键,必须依靠全身系统性的药物治疗,而千万避免手术后“一劳永逸”,“前紧后松”的错误思想。(3)目前科学研究的热点在于找到正确的靶点,区分必要或非必要接受术后辅助治疗的病人,同时也对接受辅助治疗的病人进行精准药物筛选,做到有的放矢,同病异治,这是未来的方向。2018年我们课题组构建了一个新型“打分系统”——通过“胰腺癌TNM分期系统+肿瘤分化+术前CA19-9水平”这一联合,有效区分出一部分术后不需要常规开展辅助化疗的I/II期病人,目前该项目正在实施多中心验证。2,由于目前药物研发的进展迅速,胰腺癌的治疗手段也是层出不穷,总的来说,药物联合是一个趋势:2020年国内外胰腺癌诊治指南均在之前单一化疗的基础上,推荐通过基因检测将术后辅助治疗的方式扩充至“化疗+靶向治疗+免疫治疗”的联合方式,为胰腺癌治疗的多样性和有效性增加了“利剑”。这是近期胰腺癌综合诊治的重要突破,有望在临床推广和普及。3,有效杀灭这些癌细胞的策略,除了上述一系列抗癌治疗外,更重要的是尽快恢复或提高病人抵抗力。经历了长时间麻醉,根治性大手术,和不佳饮食摄入的一系列打击下,病人虚弱的全身情况(弱抵抗力)将是癌细胞“趁虚而入”的关键。因此,提高手术质量,快速改善病人营养状况,将是抵御癌细胞扩散,早日开展辅助治疗的核心策略。一般情况下,我们建议术后4-8周,是病人接受第一轮辅助治疗的“黄金时间”。4,重视免疫治疗,提高机体免疫防御能力:(1)传统抗癌治疗如手术,放疗,化疗等,均是在“患癌土壤”上“拔除杂草”,却无法改善这一不良的体内环境(土壤)。因此提高机体免疫力,优化“土壤”质量,是维持体内稳态,避免患癌或促癌的重要因素。针对这一思路,免疫治疗被视为抗癌策略中“第四大主流治疗”,备受关注。(2)免疫治疗种类繁多,不仅仅限于目前以PD-1,PD-L1,CTLA4抗体为主的免疫检查点抑制剂,也包括各种免疫增强剂,肿瘤疫苗,细胞治疗等。但总的目的是激发人体自身潜能,“师夷长技以制夷”。(3)除药物外,丰富的营养摄入,适度的运动,健康的生活方式,积极的心态,也是维持机体稳定性必不可少的重要条件。
刘亮 主任医师 上海中山医院 普外科2241人已读 - 医学科普 2021-胰腺癌病人5年生存率首次突破两位数——10.8%
攻克“癌中之王”取得突破——2021年,胰腺癌病人的5年生存率首次突破两位数,达到10.8%。与10年前相比,几乎翻番。这是癌症学界一个少见的进步,归根结底得益于胰腺癌的综合诊治策略。 然而,胰腺癌综合诊治并非各种治疗的简单相加,它需要秉承3大理念:1,系统性疾病需要系统性诊治;2,精准分型联合同病异治;3,最合适的病人选择最合适的治疗。最终目的是:取得“1+1>2”的效果。 这将对医生的知识储备和临床操作提出了更高的要求。
刘亮 主任医师 上海中山医院 普外科6011人已读






